IVDR対応へのアプローチ
体外診断用(IVD)医療機器に関する新しい規則が2017年5月5日の欧州共同体官報(OJEC)で公布され、2017年5月26日から施行されました。
業界には、2022年5月26日から適用される新しい規則を遵守するため、5年間の移行期間があります。新しい体外診断用医療機器規則(IVDR)は、IVD機器の分類方法、ノーティファイドボディによる評価方法、ノーティファイドボディ、加盟国及び欧州委員会による承認及び規制の方法を変更する、新しい要求事項を含めた大幅な改正が行われました。本ホワイトペーパーでは、新しいIVDRの検討に焦点を当て、IVD業界に影響を及ぼす可能性がある主な変更点について概説します。IVDRは、革新を支援しながら、高水準の安全性を保証する、頑健で透明性があり、厳格で維持が可能な規制の枠組みを推奨します。この広範な改正には、101の前文、10の章、113の条項、及び15の附属書が含まれます。
新しい定義及び範囲
文書全体の変更に伴い、新しい定義が追加されました。10項目を含む合計74の定義が導入されました。新たに拡大された規則の範囲には以下の事項を含みます。
- ・情報社会サービスが提供する診断サービス
- ・遺伝子検査及び特定疾患の患者の素因に関する情報を提供するその他の検査
- ・治療に対する反応又は応答に関する情報を提供する試験
- ・機器としてのみ使用される、又は機器の一部として使用される、若しくは機器の附属品として使用されるソフトウェア。ソフトウェアは以前から規制されていましたが、リスクに基づいて分類するための規則にはずれがみられます。IVDRでは、ソフトウェアを機器として分類するための指針を明確に示しています。
- ・機器の安全性及び性能、又は機器の意図する目的に影響を与える可能性のある医療機器の部品及び構成要素
特に、本規則の適用範囲外は、以下の事項にまで拡大されています。
国際的に認証された標準物質、及び外部精度管理スキームに用いられる物質
施設内で開発された試験/機器がIVDRの下で規制されることは、興味深く注目すべき点です。医療機関がその施設内で使用するための試験キット/機器を開発する際には、施設内開発機器に固有の本指令の他の要求事項へ準拠していることに加え、ISO 15189に従った検査室品質管理システム又は国内の同等システムに準拠していることが望まれます。医療機関が試験キット/機器を他の医療機関や市場で使用できるようにする場合、その試験キット/機器はIVD機器として規制され、相手先商標製品の製造会社(OEM)によって市販される機器と同様の規則方針に従うことが望まれます。もう一つ注目すべき点は、情報社会サービスによって提供される診断サービスの要求事項であり、これは電子商取引を通じて販売される機器/サービスを本規則の対象としています。

規制当局に対する義務
本規則は、機器の規制と監視を容易にするため、医療機器調整グループ(MDCG)の設立を提案しています。
ノーティファイドボディの責任は、規則への適合を検証するために、機器の検査及びサーベイランス監査を実施するための計画を策定し、機器の物理的試験及び室内試験を実施することです。継続的な遵守を保証するためのサーベイランス監査は年に1回実施し、再評価は5年に1回実施します。さらに、ノーティファイドボディには、少なくとも5年に1回予告なしに監査を行うことが望まれています。
「ノーティファイドボディの権限」は、ノーティファイドボディの活動を監督、監視及び評価する委員会によって付与されます。機器の安全性と性能に関する規則の遵守を検証するために、加盟国は「EUリファレンス・ラボ」と呼ばれる検査所を指定することが望まれます。
EUリファレンス・ラボは、試験に加え、新規の技術、コンパニオン診断、及び機器の安全性と性能に関して専門家としての意見を提供します。
事業者に対する義務
IVDRには、製造業者がこの規則を遵守するための、具体的で新しい、詳細な要求事項を列挙しています。品質管理システム(QMS)に関連する特定の要求事項が列挙されています。技術文書、「EU適合宣言書」及び、該当する場合、関連する認証書のコピー等の、修正及び補足を含めた文書の保存期間は、EU適合宣言書(EU DOC)の適用を受けている最終機器が市場に出荷された後、少なくとも10年間となっています。それに対し、欧州指令に従って製造された最終製品の場合はわずか5年間でした。重要なこととして、製造業者は欠陥のある機器によって引き起こされた損害に対する賠償を請求する自然人又は法人に対して十分な財政的補償を提供するために、賠償責任保険に加入することが義務付けられています。製造業者は、技術文書の遵守、適合宣言、性能評価及び監視の要求事項を確実にするために、組織内で「法規制遵守の責任者」を雇用することが望まれます。零細企業及び小規模企業及び法定代理人は、そのような者を恒久的かつ継続的に自由に使えなければなりません(必ずしも組織内で雇用される必要はありません)。
輸入業者及び販売業者への要求事項は厳しくなりました。これらの事業者が遵守しなければならない注目すべき変更のいくつかは、これらに限定されるものではありませんが、以下のことを保証することが望まれています。
- ・機器にはCEマークが付与され、EU DOCが利用可能であること
- ・製造業者が特定され、法定代理人(該当する場合)が指定されていること
- ・ラベル表示され、該当する場合はUDIが利用可能であること
- ・市販後調査及び苦情処理に積極的に参加すること
- ・機器の意図する目的を損なうことのない保管及び輸送のための処理を行うこと
- ・製造業者が賠償責任保険に加入していること
機器の意図する目的を変更した後、又は機器の遵守状況を損なう機器の変更をした後に、機器が輸入業者/販売業者のブランド名又は登録商標名又は登録商標を付して市場で販売された場合、製造業者の義務は、輸入業者/販売業者に適用されます。
意図する目的を変更することなく、既に市場で販売されている機器を個々の患者のために組立てたり、個人に合わせて修正したりする事業体、又は製造業者がラベル上の製造業者として特定され、本規則を遵守する責任を負うことについて製造業者と合意した事業体は、本条項の除外を主張することができます。
輸入業者/販売業者は、このような活動を実施するためにQMSを構築しておくことが望まれます。機器の意図する目的に影響を与えずに機器の変更を行った場合は、機器を市場で販売する28日前に、製造業者及び加盟国の規制当局に再包装/ラベルの付け替えの情報を通知しなければなりません。
欧州指令における種々の条項での法定代理人の要求事項は、新しい条項に記載されています。また、MEDDEV 2.5/10(2012年1月)の要求事項も組み込まれました。法定代理人の変更に関する新しい要求事項も記載されています。

医療機器個体識別子及びトレーサビリティ
製造業者は、国際的に認められた医療機器の識別及びコード化の規格により作成された数字又は英数字からなる医療機器個体識別子(UDI)を割り当て、維持しなければなりません。UDIは、ライフサイクル、すなわち製造、包装、流通から使用までの全期間を通して、表示され維持されなければなりません。すべての機器は、市場で販売する前に、機器のラベル及び上位レベルの全ての梱包、適用宣言書及び技術文書にUDIを付けなければなりません。クラスB、クラスC、及びクラスDの機器の場合、製造業者は、ノーティファイドボディに申請する前にUDIを指定しなければなりません。
機器の電子登録が導入され、すべての製造業者は、機器を市場で販売する前に電子登録し、既存の機器のデータベースを移行期間中に更新することが必須となります。ノーティファイドボディに関わる機器は、ノーティファイドボディに申請する前に登録することが望まれます。附属書VIのパートAのセクション1に記載されている登録に必要な項目の新しいリストには以下を含みますが、これに限定されるものではありません。
自己検査用やベッドサイド検査用に関わらず、機器の意図する目的に関する明確な表示
ヒト/動物/生物由来の組織、細胞、又はその誘導体の存在
クラスC及びクラスDの安全性及び性能の概要 - 第29条にこれに対する要求事項のリストが提供されています。
電子登録で提供される詳細の変更は、1週間以内に更新されることが望まれます。情報提供後1年以内、その後2年ごとに、事業者はデータが正確であることを確認しなければなりません。本規則は、Eudamedと呼ばれるデータベースで公開される、安全性と性能の評価報告書を含むデータのリストも要求しています。本規制により、Eudamedでどの文書をどの段階で利用可能にすべきかが明確に示されています。
IVDRではサプライチェーンの要求事項が精査されており、EU適合宣言書の適用を受けている最終機器が市場で販売されてから少なくとも10年間は、事業者が規制当局に以下を明らかにするためのプロセスを整備することが要求されます。
- ・機器を直接供給した事業者
- ・機器を直接供給された事業者
- ・機器を直接供給した医療機関又は医療従事者
分類及び適合性評価
10の実施規則と7つのクラス分類規定により、新しいリスクに基づく分類が導入されました。機器はA、B、C、及びDに分類されます。IVD指令(IVDD)では、ほとんどのIVDはノーティファイドボディの関与を必要とせず、自己認証されていました。
新しい分類システムでは、製品の80%近くがクラスB、C、及びDに分類され、これらのクラスには、ノーティファイドボディの関与が必要です。すべての国/地域の市販前承認のための一貫したアプローチを確立するため、製造業者は、IVDRの附属書IXから附属書XIに記載されている機器クラスと適合性評価手順に適用される相互関係を図で示し、従わなければなりません。
リスクマネジメントは、附属書Iに従った一般的な安全性と必須要求事項の一部として実行され利用できるようにしなければなりません。リスクマネジメントは、製品のライフサイクルを通して随時更新文書として維持されることが望まれます。
クラスD機器に対する追加の審査も確立されています。クラスD機器もバッチ検証を受けなければなりません。EUリファレンス・ラボは、要求されている性能及び機器の共通仕様(CS)への適合、及び整合規格及び附属書Iの要求事項(一般的な安全性及び性能の要求事項)への適合を検証するために採用されています。さらに、新規の技術に関して、EUリファレンス・ラボは、ノーティファイドボディによる評価の前に、専門家としての意見が求められます。
製造業者は、IVDRの要求事項を満たすクラスA製品の適合宣言書を作成することができます。
しかし、滅菌装置については附属書IX又は附属書XIの要求事項が適用可能であり、ノーティファイドボディの関与は機器の滅菌条件の設定、確保及び維持に関連する側面に限定されます。自己検査及びベッドサイド検査は、附属書Xに記載されている要求事項に従います。コンパニオン診断機器はすべてクラスCと見なされ、ノーティファイドボディによる監視が必要です。ノーティファイドボディによる適合性評価に加えて、承認には指令2001/83/ ECに従って加盟国によって指定された欧州医薬品機関(EMA)又は規制当局との協議が必要です。
性能評価及び市販後調査
新しい規則では、必須の市販後性能フォローアップ(「PMPF」)計画及び定期的安全性最新報告(「PSUR」)を含む、性能評価及び臨床的エビデンスに関連する概念を取り入れています。性能評価を確立するために、製造業者は機器の科学的妥当性、分析性能及び臨床性能(該当する場合)を実証する義務があり、これは機器のライフサイクルを通して更新されなければなりません。
製造業者は、クラスC及びクラスDの安全性と性能の要約報告書を少なくとも年1回更新する必要があります。IVDRは、他の情報源に依拠することが正当化されない限り、臨床的エビデンスを確立するための性能試験を要求します。製造業者は、クラスA及びクラスBの機器の市販後調査の分析の結果と結論をまとめた市販後調査実施報告書を更新しなければなりません。クラスC及びクラスDの機器の製造業者は少なくとも年1回PSURを更新し、電子システムによって提出しなければなりません。
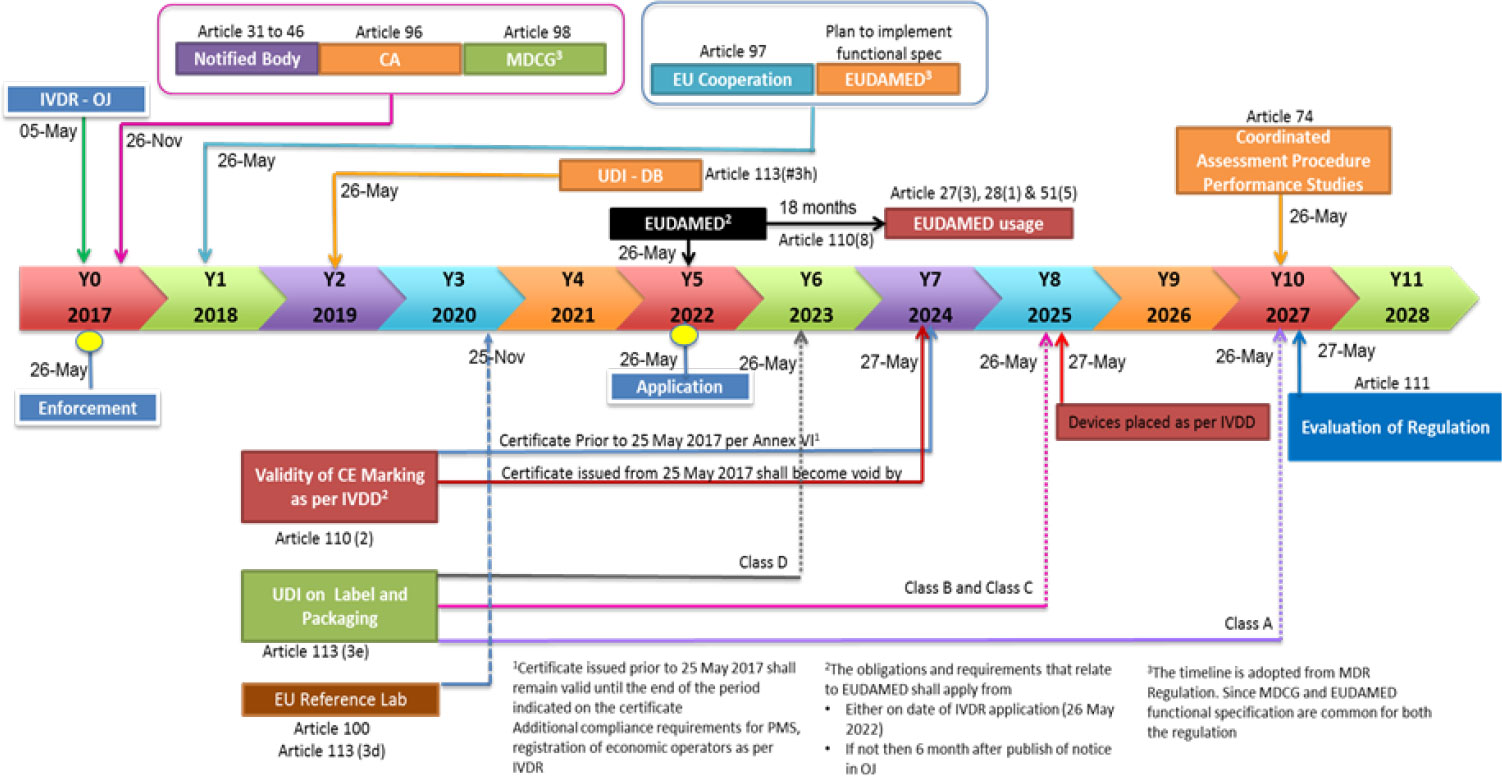
移行のタイムライン
本規則は、正式に採択され、2017年5月27日に施行されます。公布された規則は、その後5年間の移行期間に続き、2022年5月26日から完全に適用されます。2017年5月25日より前に発行された適合証明書(認証書に記載された期間まで有効)は、2017年5月25日から発行されたEC検証書及び証明書に従い、2024年5月27日までに無効になります。ただし、事業者の登録、市販後調査及びQMSに関連する要求事項は適用されます。
ラベルとパッケージのUDIのタイムラインも規定されています。クラスD機器の場合、UDIは2023年5月26日以前に実施しなければなりません。クラスB及びクラスCの場合、期限は2025年5月26日であり、クラスAの期限は2027年5月26日です。移行のタイムラインの図に、製造業者に関するさまざまな規制活動及び義務について提案されたタイムラインを明確に示しています。
結論
製造業者及びその他の事業者にとって、IVDRを検討し、影響評価を実施する計画を策定するために移行戦略を構築することは重要です。
確実に管理を行い、新しい要求事項を実現するために、下請け業者及び供給業者との合意形成をすべきです。ノーティファイドボディが規制当局の権限及び評価の下に置かれたため、規制当局が認定ノーティファイドボディのリストを公表するまで、製造業者は、既存のノーティファイドボディを継続するか、別のノーティファイドボディに切り替えることが求められます。
臨床的エビデンスに関する新しく厳格な要求事項により、業界内にはすでに混乱が生じています。製造業者は、既存の証拠を検討し、それがIVDRによって設定された新しい定義と性能評価の要求事項に準拠していることを確認することが必要となります。
何より、欧州委員会からのMED DEVのような分類規則及びコンパニオン診断のガイダンス文書により、業界には実際に利益がもたらされるでしょう。
2022年5月27日以降これらの課題が事実上のものとなり、IVDRに準拠していない製造業者はEU内で自社製品を販売することができない可能性があります。
HCLは、規制関連のコンサルタントを幅広く抱え、必要な期間内の変更に対応するために、業界に対する専門的なサービスの提供に取り組んでいます。